由国家直接受理此前,各省的保健品申报都需要地方相关部门初审,对此,谢晓于表示,由于省级药监部门改革要到明年初才到位,为了不影响申报工作,暂由国家直接受理。但她强调,不需要地方初审并不等于取消初审。由SFDA直接接受初审。
明年启动相关法规修订工作
谢晓于透露,明年初修订完善保健食品的有关法规工作将启动。SFDA为完善法规将进行全面调研。另外,SFDA还将就保健食品批号换证摸底普查。过去的“卫食健字”转由SFDA审批后文号改为“国食健字”。
批文申报流程保健食品申报主要涉及以下四种机构:
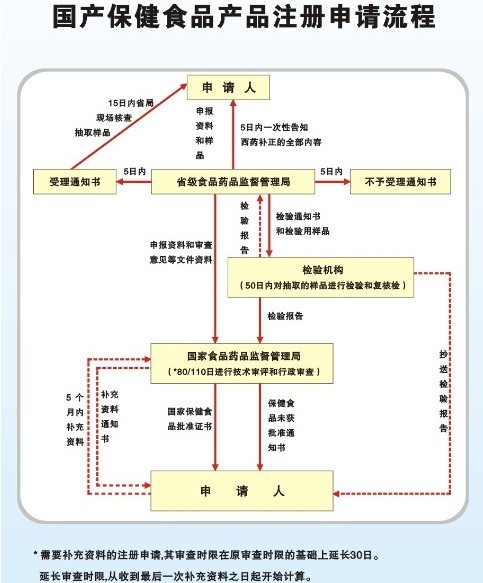
国食健字批文申办流程
检测机构:接受企业的委托,负责对产品进行技术检验,并出具检验报告。具体为各省、直辖市的疾病控制中心(或卫 生防疫站) 、中国 CDC 食品卫生监督检验所、中国预防医学科学院、以及部分医学院校。
受理办:包括省药监局受理处和国家药监局保健食品评审中心。负责对企业的申报材料进行初步审核,材料符合要求则,负责安排产品参加评审会;将评审意见通知企业;对于拟批准的产品上报行政部门审批;发放证书等。
评审委员会:国家药监局保健食品评审中心同时负责组织专家对申报的产品进行技术评审。
行政部门:国家药监局注册司对评审委员会技术评审的产品进行审核,如符合有关法规的规定,则予以批准。[1]
保健食品,系指具有特定保健功能的食品,即适用于特定人群食用,具有调节机体功能,不以治疗为目的的食品。所以欲注册保健食品的产品,必须具有三种属性:
①食品属性;
②功能属性,具有特定的功能;
③非药品属性。
保健食品注册,是指国家食品药品监督管理局根据申请人的申请,依照法定程序、条件和要求,对申请注册的保健食品的安全性、有效性、质量可控性以及标签说明书内容等进行系统评价和审查,并决定是否准予其注册的审批过程;包括对产品注册申请、变更申请和技术转让产品注册申请的审批。
保健食品主要分为营养素补充剂和具有调节机体功能的功能性产品。
(1)营养素补充剂:指以补充一种或多种维生素、矿物质而不以提供能量为目的的产品。其作用是补充膳食供给的不足,预防营养缺乏和降低发生某些慢性退行性疾病的危险性。此类产品仅限于补充维生素和矿物质。
(2)国家食品药品监督管理局公布的保健食品的27种功能:(申请功能数量不受限制)
1、增强免疫力功能 | 15、抗氧化功能★ |
2、改善睡眠功能 | 16、辅助改善记忆功能★ |
3、对化学性肝损伤有辅助保护功能 | 17、促进排铅功能★ |
4、增加骨密度功能 | 18、清咽功能★ |
5、提高缺氧耐受力功能 | 19、辅助降血压功能★ |
6、对辐射危害有辅助保护功能 | 20、促进泌乳功能★ |
7、缓解体力疲劳功能◇ | 21、减肥功能★◇ |
8、缓解视疲劳功能 ☆ | 22、改善生长发育功能★◇ |
9、祛痤疮功能 ☆ | 23、改善营养性贫血功能★ |
10、祛黄褐斑功能 ☆ | 24、调节肠道菌群功能★ |
11、改善皮肤水份功能 ☆ | 25、促进消化功能★ |
12、改善皮肤油份功能 ☆ | 26、通便功能★ |
13、辅助降血脂功能★ | 27、对胃黏膜损伤有辅助保护功能★ |
14、辅助降血糖功能★ |
注:标有★的功能,既需要进行动物功能试验又需要进行人体功能试验。
标有☆功能,只需进行人体功能试验,无需进行动物功能试验。
标有◇的项目需做兴奋剂检测。
拟申请的功能不在以上公布的27种范围内的,申请人应当自行进行动物试验和人体试食试验,并向确定的检验机构提供功能研发报告。
保健食品注册工作程序
检验 ——> 受理 ——> 初审 ——> 终审 ——> 批准
保健食品评审会的召开频率
保健食品评审大会每个月召开一次,一般于月中旬或下旬开始,历时约10~15天。小会随时召开。
保健食品都要检验哪些项目?
注册保健食品一般要进行安全性毒理学试验、功能学试验、功效成分或标志性成分检测、卫生学试验、稳定性试验。
注册国产保健食品需要提供什么资料?
一、保健食品注册申请表。
二、申请人身份证、营业执照或者其它机构合法登记证明文件的复印件。
三、提供申请注册的保健食品的通用名称与已经批准注册的药品名称不重名的检索材料(从国家食品药品监督管理局政府网站数据库中检索)。
四、申请人对他人已取得的专利不构成侵权的保证书。
五、提供商标注册证明文件(未注册商标的不需提供)。
六、产品研发报告(包括研发思路,功能筛选过程,预期效果等)。
七、产品配方(原料和辅料)及配方依据;原料和辅料的来源及使用的依据。
八、功效成分/标志性成分、含量及功效成分/标志性成分的检验方法。
九、生产工艺简图及其详细说明和相关的研究资料。
十、产品质量标准及其编制说明(包括原料、辅料的质量标准)。
十一、直接接触产品的包装材料的种类、名称、质量标准及选择依据。
十二、检验机构出具的试验报告及其相关资料,包括:
1、试验申请表;
2、检验单位的检验受理通知书;
3、安全性毒理学试验报告;
4、功能学试验报告;
5、兴奋剂、违禁药物等检测报告(注册缓解体力疲劳、减肥、改善生长发育功能的注册申请);
6、功效成份检测报告;
7、稳定性试验报告;
8、卫生学试验报告;
9、其他检验报告(如:原料鉴定报告、菌种毒力试验报告等)。
十三、产品标签、说明书样稿。
十四、其它有助于产品评审的资料。
十五、两个未启封的最小销售包装的样品。
注:
1、以真菌、益生菌、核酸、酶制剂、氨基酸螯合物等为原料的产品的注册申请,除提供上述资料外,还必须按照有关规定提供相关的申报资料。
2、以国家限制使用的野生动植物为原料的产品的注册申请,除提供上述资料外,还必须提供政府有关主管部门出具给原料供应方的允许该原料开发、利用的证明文件以及原料供应方和申请人签订的购销合同。
3、以补充维生素、矿物质为目的保健食品的注册申请,不需提供动物功能评价试验报告和/或人体试食试验报告和功能研发报告。
4、注册的功能不在国家食品药品监督管理局公布的功能项目范围内的,除根据使用原料的情况提供上述资料外,还必须提供以下与新功能相关的资料:(1)功能研发报告:包括功能名称、申请的理由和依据、功能学评价程序和检验方法以及研究过程和相关数据、建立功能学评价程序和检验方法的依据和科学文献资料等。(2)申请人依照该功能学评价程序和检验方法对产品进行功能学评价试验的自检报告。(3)确定的检验机构出具的依照该功能学评价程序和检验方法对产品进行功能学评价的试验报告以及对检验方法进行评价的验证报告。
5、同一申请人申请同一个产品的不同剂型的注册,如果其中的一个剂型已经按照规定进行了全部试验,并且检验机构已经出具了试验报告,其他剂型的注册可以免作功能学和安全性毒理学试验,但必须提供已经进行过的功能学和安全性毒理学试验的试验报告的复印件。工艺有质的变化,影响产品安全、功能的除外。
保健食品的标签与说明书的相关规定
答:申请注册的保健食品标签、说明书样稿的内容应当包括产品名称、主要原(辅)料、功效成分/标志性成分及含量、保健功能、适
宜人群、不适宜人群、食用量与食用方法、规格、保质期、贮藏方法和注意事项等。
经批准生产上市的保健食品标签应当符合国家有关规定。
上一条: GMP认证相关文件
下一条: 安全购买保健品四个注意事项
广州靓源生物科技有限公司 版权所有
客服电话:周经理18530956538
地址:广州市萝岗区高新技术产业开发区科丰路81号